Онкорадиология, лучевая
диагностика и терапия
диагностика и терапия






МАТЕРИАЛЫ
КТ и МРТ



МАТЕРИАЛЫ
КТ и МРТ


















СОДЕРЖАНИЕ
СТАНДАРТЫ ПРОВЕДЕНИЯ ИССЛЕДОВАНИЙ
МРТ головы
МРТ позвоночника и спинного мозга
КТ органов брюшной полости
МРТ органов брюшной полости


КЛАССИФИКАЦИИ

LI-RADS
по данным МРТ
O-RADS

VI-RADS
PI-RADS




МРТ органов малого таза у женщин
МРТ органов малого таза
при подозрении на рак предстательной железы
МРТ органов малого таза
при подозрении на опухоли прямой кишки и анального канала
КТ костно-мышечной системы




МРТ костно-мышечной системы




по данным МРТ
BI-RADS
RECIST 1.1















СОДЕРЖАНИЕ
СТАНДАРТЫ ПРОВЕДЕНИЯ ИССЛЕДОВАНИЙ
КЛАССИФИКАЦИИ

LI-RADS

VI-RADS
МРТ позвоночника и спинного мозга

МРТ головы

КТ органов брюшной полости

МРТ органов брюшной полости

МРТ органов малого таза
при подозрении на рак предстательной железы

МРТ органов малого таза у женщин

МРТ органов малого таза
при подозрении на опухоли прямой кишки и анального канала

КТ костно-мышечной системы

МРТ костно-мышечной системы

по данным МРТ
O-RADS

PI-RADS


по данным МРТ
BI-RADS
RECIST 1.1

МРТ ГОЛОВЫ




Стандартный протокол нативного исследования головного мозга:
- Аксиальные Т2-ВИ TSE/FSE (Turbo/Fast Spin Echo).
- Коронарные Т2-ВИ TSE/SE.
- Аксиальные Т2-ВИ FLAIR.
- Аксиальные DWI b = 0 и b = 1 000 с построением ИКД-карт.
- 3D Т1-ВИ с последующим восстановлением изображений в 3 ортогональных проекциях (возможно выполнение Т1-ВИ TSE/FSE в аксиальной и сагиттальной проекциях).
- Аксиальные SWI, SWAN (опционально).
- Внутривенное введение экстрацеллюлярных ГМРКС: Т2*-перфузия (опционально).
- 3D Т1-ВИ MPRAGE или 3D Т1-ВИ с последующим восстановлением изображений в 3 ортогональных проекциях (возможно выполнение Т1-ВИ TSE/FSE в аксиальной, коронарной и сагиттальной проекциях).
- Аксиальные Т2-ВИ FLAIR (опционально).
Рис. 1. Пациентка П. 45 лет. Метастазы гранулезно-клеточной опухоли яичников в головном мозге. МРТ-исследование головного мозга в аксиальных проекциях. При нативном исследовании на Т2ВИ (а–в) и Т1ВИ (г–е) признаков метастатического процесса не выявлено. После введения ГМРКС (ж–и) определяются множественные очаги накопления ГМРКС (стрелки), которые являются отображением метастатического поражения
Рис. 2. Пациентка Ш. 62 лет. Глиома головного мозга. МРТ-исследование головного мозга в аксиальных проекциях. При нативном исследовании на Т2ВИ(а) и Т1ВИ (б) в левой лобной доле определяется крупная опухоль без четких границ с инфильтративным распростра- нением на правую лобную долю и перифокальным отеком (стрелки). После внутивенного введения ГМРКС (в) границы опухоли дифференцируются в виде гиперинтенсивной каймы (стрелка)
Материал подготовила: к.м.н. Лаптева М.Г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Введение ГМРКС показано всем пациентам с подозрением на опухолевое поражение вещества и оболочек головного мозга как первичной, так и вторичной (метастатической) этиологии.
Введение ГМРКС при первичных опухолях головного мозга позволяет провести дифференциальную диагностику, оценить степень злокачественности, более точно определить объём и границы опухоли на фоне перифокального отёка. При метастатическом поражении введение ГМРКС является решающим этапом при оценке распространённости заболевания, при дифференциальной диагностике вторичных и различных неопухолевых изменений. Всё это имеет принципиальное значение при выборе тактики лечения пациента: определения возможности и объёма оперативного вмешательства, выборе плана химиотерапии и лучевой терапии. В дальнейшем использование в/в контрастирования применяется для оценки эффективности проведённого лечения.
1
2
3
1
2
3
4
5
6
7
8
9

МРТ ПОЗВОНОЧНИКА И СПИННОГО МОЗГА


Стандартный протокол нативного исследования позвоночника и спинного мозга:
- Сагиттальные Т2-ВИ TSE.
- Коронарные Т2-ВИ TSE.
- Аксиальные Т2-ВИ (только в зоне интереса).
- Коронарные Т2-ВИ TSE с подавлением сигнала жировой ткани или STIR.
- Сагиттальные Т1-ВИ TSE/SE или TIR. В/в введение экстрацеллюлярных ГМРКС:
- Сагиттальные Т1-ВИ TSE/SE или Т1-ВИ TIR/FLAIR.
- Коронарные Т1-ВИ TSE/SE или Т1-ВИ TIR/FLAIR.
- Аксиальные Т1-ВИ TSE/SE или Т1-ВИ TIR/FLAIR (только в зоне интереса).
Рис. 1. Пациент С. 60 лет. Доброкачественная опухоль оболочек спинного мозга. МРТ- исследование нижнегрудного отдела позвоночника в сагиттальных (а–в) и фронтальной (г) проекциях. При нативном исследовании на Т2 ВИ (а) и Т1 ВИ (б) в позвоночном канале на уровне межпозвонкового диска Th11–12 выявляется объемное узловое образование, контуры которого сливаются с медуллярным веществом спинного мозга (стрелки). После введения ГМРКС признаков вовлечения медуллярного вещества спинного мозга (в, г) не обнаружено (стрелки).
Материал подготовила: к.м.н. Лаптева М.Г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Вместо пунктов Е–З может быть выполнено 3D Т1-ВИ – сверхбыстрое градиентное эхо с изотропным разрешением и последующим восстановлением изображений в 3 ортогональных проекциях.
Применение ГМРКС в диагностике изменений спинного мозга также необходимо для выявления патологических изменений, проведения дифференциального диагноза между первичными, метастатическими и различными неопухолевыми изменениями, а также при необходимости оценки эффективности проведённого лечения. Кроме того, введение ГМРКС улучшает визуализацию межпозвонковых дисков, пре- и паравертебральных мягких тканей.
Применение ГМРКС в диагностике изменений спинного мозга также необходимо для выявления патологических изменений, проведения дифференциального диагноза между первичными, метастатическими и различными неопухолевыми изменениями, а также при необходимости оценки эффективности проведённого лечения. Кроме того, введение ГМРКС улучшает визуализацию межпозвонковых дисков, пре- и паравертебральных мягких тканей.
1
2
3
4
КТ-ИССЛЕДОВАНИЕ ОРГАНОВ БРЮШНОЙ ПОЛОСТИ

КТ-исследования в абдоминальной области, в подавляющем большинстве случаев, необходимо выполнять с внутривенным контрастированием с применением РКС.
Показания к выполнению нативного КТ-исследования довольно ограничены, существует ряд причин, обуславливающих необходимость ее проведения:
Таким образом, внутривенное контрастирование при исследовании области живота следует выполнять во всех случаях, если не имеется серьезных противопоказаний к применению РКС
Методика исследования
КТ в диагностике опухолей органов брюшной полости и забрюшинной локализации обладает достаточно широким диапазоном возможностей и применяется для:
КТ в выявлении и дифференциальной диагностике доброкачественных и злокачественных новообразований органов брюшной полости и забрюшинной локализации
Выявление и дифференциальная диагностика новообразований печени, почек и поджелудочной железы основаны на оценке их структуры и характера васкуляризации, гемодинамических особенностей опухолей. Наиболее значимые результаты при этом достигаются путем сравнения данных, полученных в нативную фазу до начала введения контрастного средства, с двумя последующими фазами исследования (артериальной и венозной), в ряде случаев с отсроченной фазой спустя 5–10 мин.
Около 30% выявляемых очаговых образований печени, таких как гепатоцеллюлярный рак, некоторые метастазы, фокальная узловая гиперплазия и пр., являются гиперваскулярными и лучше визуализируются именно в артериальную фазу исследования. В венозную фазу (спустя 40–60 сек. от начала внутривенного введения РКС) наиболее отчетливо выявляются гиповаскулярные новообразования, подавляющее большинство которых составляют метастазы различных первичных опухолей. В эту фазу происходит максимальное усиление паренхимы печени, на фоне которой подобные образования визуализируются более отчетливо. Отсроченная фаза (спустя 5 мин. после начала введения РКС) используется, как правило, для дифференциальной диагностики выявляемых очаговых образований в печени, например метастазов и гемангиом.
Показания к выполнению нативного КТ-исследования довольно ограничены, существует ряд причин, обуславливающих необходимость ее проведения:
- визуализация конкрементов/кальцинатов и кровоизлияний в очагах;
- идентификация жировой дистрофии печени;
- противопоказания к применению РКС.
Таким образом, внутривенное контрастирование при исследовании области живота следует выполнять во всех случаях, если не имеется серьезных противопоказаний к применению РКС
Методика исследования
- Нативное сканирование области живота на односрезовых аппаратах выполняется срезами 5–10 мм, шагом стола 7–12 мм с индексом реконструкции 5–10 мм. На многосрезовых томографах исследование может проводиться при меньшей величине коллимации. В частности, 4-срезовые аппараты позволяют уменьшить коллимацию до 2,5 мм, 16-срезовые и более мощные аппараты создают условия для субмиллиметрового сканирования, при котором величина коллимации достигает 0,6 мм.
- После внутривенного введения контрастного средства выполняются повторные серии сканирований в артериальную, венозную и отсроченную фазы исследования (при исследовании почек оцениваются кортикомедуллярная, нефрографическая и выделительная фазы).
- В качестве контрастного средства целесообразно использовать неионные РКС в объеме 70–120 мл (в зависимости от веса пациента) при концентрации йода 300–400 мг/мл.
- Методика исследования может быть основана на фиксированной задержке между началом инъекции контрастного препарата и началом сканирования. При этом используется усредненное время прохождения болюса через зону интереса при введении контрастного средства в локтевую вену. Для получения артериальной фазы контрастного усиления сканирование следует начинать спустя 20–28 секунд (при скорости 2,5–3 мл/сек., соответственно) после начала введения контрастного средства. Для получения венозной фазы – спустя 60–70 сек. Отсроченная фаза исследования выполняется через 5–10 мин. При использовании тестового болюса время задержки определяется после пробного введения 10–15 мл контрастного средства и предварительного динамического сканирования. Современные многосрезовые аппараты позволяют автоматически определять время начала сканирования. Для этого в программах типа CARE Bolus на аксиальном срезе выбирается зона интереса, обычно внутри изображения брюшной аорты, после чего начинаются синхронное введение контрастного средства и динамическое сканирование. При достижении порога плотности (обычно 100–150 HU) динамическое сканирование автоматически прекращается, стол перемещается в исходное положение, и начинается спиральное сканирование выбранной зоны.
- Отдельным пациентам, перенесшим многократные инъекции химиопрепаратов, следует снизить скорость введения контрастного средства до 1,8–2,0 мл/сек. ввиду повышенной опасности разрыва поврежденных венозных сосудов. При введении контрастного средства через подключичный катетер скорость не ограничена.
КТ в диагностике опухолей органов брюшной полости и забрюшинной локализации обладает достаточно широким диапазоном возможностей и применяется для:
- выявления и дифференциальной диагностики доброкачественных и злокачественных новообразований органов брюшной полости и забрюшинной локализации;
- стадирования опухолевого процесса, оценки местного и отдаленного распространения;
- в оценке эффективности противоопухолевого лекарственного лечения.
КТ в выявлении и дифференциальной диагностике доброкачественных и злокачественных новообразований органов брюшной полости и забрюшинной локализации
Выявление и дифференциальная диагностика новообразований печени, почек и поджелудочной железы основаны на оценке их структуры и характера васкуляризации, гемодинамических особенностей опухолей. Наиболее значимые результаты при этом достигаются путем сравнения данных, полученных в нативную фазу до начала введения контрастного средства, с двумя последующими фазами исследования (артериальной и венозной), в ряде случаев с отсроченной фазой спустя 5–10 мин.
Около 30% выявляемых очаговых образований печени, таких как гепатоцеллюлярный рак, некоторые метастазы, фокальная узловая гиперплазия и пр., являются гиперваскулярными и лучше визуализируются именно в артериальную фазу исследования. В венозную фазу (спустя 40–60 сек. от начала внутривенного введения РКС) наиболее отчетливо выявляются гиповаскулярные новообразования, подавляющее большинство которых составляют метастазы различных первичных опухолей. В эту фазу происходит максимальное усиление паренхимы печени, на фоне которой подобные образования визуализируются более отчетливо. Отсроченная фаза (спустя 5 мин. после начала введения РКС) используется, как правило, для дифференциальной диагностики выявляемых очаговых образований в печени, например метастазов и гемангиом.
КТ в стадировании опухолевого процесса, оценке местного и отдаленного распространения
Широкое применение КТ в стадировании онкологических новообразований прежде всего обусловлено возможностью одновременного выполнения нескольких зон исследования, мультипланарных реконструкций, немаловажным является то, что прекрасная анатомическая визуализация сосудистых структур лимфоколлекторов, паренхиматозных органов и костей позволяет использовать метод как в оценке местного распространения опухоли, так и ее отдаленного метастазирования.
Рак желудка
Всем пациентам с диагнозом рак желудка рекомендуется выполнять КТ грудной клетки, брюшной полости и малого таза с внутривенным с использованием неионных йодсодержащих препаратов и пероральным контрастированием для оценки распространенности опухолевого процесса и планирования лечения.
Рак ободочной кишки
Всем пациентам с диагнозом рак ободочной кишки рекомендуется выполнять КТ органов грудной и брюшной полости с внутривенным контрастированием с использованием неионных йодсодержащих препаратов.
В протоколе КТ следует отражать: расстояние от края опухоли до наиболее близкого анатомического ориентира (купола слепой кишки, печеночного/селезеночного изгиба или анального отверстия), протяженность опухоли вдоль кишечной стенки, наличие инвазии в мезоколон и ее глубину, наличие инвазии в брюшину, наличие лимфатических узлов мезоколона и забрюшинного пространства с признаками метастатического поражения и их размеры, наличие отдаленных метастазов, локализованных по брюшине и во внутренних органах.
Для оценки резектабельности метастазов колоректального рака в печени предпочтительна МРТ органов брюшной полости с внутривенным контрастированием. Пациентам с противопоказаниями к проведению МРТ рекомендуется выполнение КТ с внутривенным контрастированием. МРТ обладает наиболее высокой чувствительностью по сравнению с другими диагностическими методами, в особенности в отношении метастазов размером <1 см. Не допускается планирование резекции метастазов на основании только данных УЗИ печени или КТ без внутривенного контрастирования.
Рак поджелудочной железы
Всем пациентам с диагнозом рак поджелудочной железы рекомендуется выполнять КТ грудной клетки, брюшной полости и малого таза с внутривенным контрастированием с использованием неионных йодсодержащих препаратов для оценки распространенности опухолевого процесса и планирования лечения.
Исследование брюшной полости должно проводиться строго с внутривенным болюсным контрастированием по разработанному для оценки поджелудочной железы протоколу:
Протокол описания КТ-исследования должен включать:
1) степень вовлечения верхней брыжеечной артерии (протяженность инфильтрации, степень вовлечения более или менее 180°);
2) степень вовлечения чревного ствола и/или его ветвей (протяженность инфильтрации, степень вовлечения более или менее 180°), вовлечение гастродуоденальной артерии;
3) степень вовлечения воротной вены и верхней брыжеечной вены (протяженность, наличие венозных коллатералей, степень проходимости в зоне инфильтрации, наличие и локализация опухолевого и/или кровяного тромба);
4) степень вовлечения селезеночной вены (протяженность, наличие венозных коллатералей, степень проходимости в зоне инфильтрации, наличие и локализация опухолевого и/или кровяного тромба);
5) указывается степень расширения внепеченочных желчных протоков, главного панкреатического протока с указанием уровня блока.
Рак паренхимы почки
Всем пациентам с диагнозом рак почки рекомендуется выполнять КТ брюшной полости с внутривенным контрастированием с использованием неионных йодсодержащих препаратов для оценки распространенности опухолевого процесса и планирования лечения. Пациентам с подтвержденным диагнозом почечно-клеточный рак стадии ≥ cT1b и/или cN1 рекомендуется проведение КТ органов грудной клетки.
Протокол мультидетекторной КТ включает нативную фазу, кортикомедуллярную фазу (через 40 сек. после начала введения контрастного препарата), нефрографическую фазу (через 90 сек. после начала введения контрастного препарата) и урографическую фазу (через 7 мин. после введения контрастного препарата).
Рекомендуемая толщина реконструированного среза КТ должна составлять 1–3 мм. Трехмерная КТ-реконструкция отображает анатомию сосудов почки, взаимоотношение почечной паренхимы и новообразования, а также помогает планировать хирургический доступ, объем и ход оперативного вмешательства.
Использование стандартизованных объективных и воспроизводимых нефрометрических шкал (RENAL, PADUA) нивелирует вариабельность трактовки результатов визуализации разными специалистами. Нефрометрические показатели могут предсказать ожидаемую техническую сложность резекции почки и коррелируют с длительностью ишемии, операционным временем, объемом кровопотери, частотой осложнений и вероятностью перехода от резекции почки к радикальной нефрэктомии. Нефрометрические шкалы могут помочь в принятии клинических решений в отношении объема операции и хирургического доступа.
Широкое применение КТ в стадировании онкологических новообразований прежде всего обусловлено возможностью одновременного выполнения нескольких зон исследования, мультипланарных реконструкций, немаловажным является то, что прекрасная анатомическая визуализация сосудистых структур лимфоколлекторов, паренхиматозных органов и костей позволяет использовать метод как в оценке местного распространения опухоли, так и ее отдаленного метастазирования.
Рак желудка
Всем пациентам с диагнозом рак желудка рекомендуется выполнять КТ грудной клетки, брюшной полости и малого таза с внутривенным с использованием неионных йодсодержащих препаратов и пероральным контрастированием для оценки распространенности опухолевого процесса и планирования лечения.
Рак ободочной кишки
Всем пациентам с диагнозом рак ободочной кишки рекомендуется выполнять КТ органов грудной и брюшной полости с внутривенным контрастированием с использованием неионных йодсодержащих препаратов.
В протоколе КТ следует отражать: расстояние от края опухоли до наиболее близкого анатомического ориентира (купола слепой кишки, печеночного/селезеночного изгиба или анального отверстия), протяженность опухоли вдоль кишечной стенки, наличие инвазии в мезоколон и ее глубину, наличие инвазии в брюшину, наличие лимфатических узлов мезоколона и забрюшинного пространства с признаками метастатического поражения и их размеры, наличие отдаленных метастазов, локализованных по брюшине и во внутренних органах.
Для оценки резектабельности метастазов колоректального рака в печени предпочтительна МРТ органов брюшной полости с внутривенным контрастированием. Пациентам с противопоказаниями к проведению МРТ рекомендуется выполнение КТ с внутривенным контрастированием. МРТ обладает наиболее высокой чувствительностью по сравнению с другими диагностическими методами, в особенности в отношении метастазов размером <1 см. Не допускается планирование резекции метастазов на основании только данных УЗИ печени или КТ без внутривенного контрастирования.
Рак поджелудочной железы
Всем пациентам с диагнозом рак поджелудочной железы рекомендуется выполнять КТ грудной клетки, брюшной полости и малого таза с внутривенным контрастированием с использованием неионных йодсодержащих препаратов для оценки распространенности опухолевого процесса и планирования лечения.
Исследование брюшной полости должно проводиться строго с внутривенным болюсным контрастированием по разработанному для оценки поджелудочной железы протоколу:
- без перорального контрастирования рентгеноконтрастными йодсодержащими веществами;
- объем контрастного препарата из расчета 1–1,2 мл/кг при плотности контрастного вещества 350 мг йода/мл, скорость введения КВ от 3 мл/сек.;
- артериальная фаза на 20–35 секундах (от момента введения контрастного препарата)
- венозная фаза на 60-80 секундах (от момента введения контрастного препарата);
- отсроченная фаза на 5–10 минуте.
Протокол описания КТ-исследования должен включать:
1) степень вовлечения верхней брыжеечной артерии (протяженность инфильтрации, степень вовлечения более или менее 180°);
2) степень вовлечения чревного ствола и/или его ветвей (протяженность инфильтрации, степень вовлечения более или менее 180°), вовлечение гастродуоденальной артерии;
3) степень вовлечения воротной вены и верхней брыжеечной вены (протяженность, наличие венозных коллатералей, степень проходимости в зоне инфильтрации, наличие и локализация опухолевого и/или кровяного тромба);
4) степень вовлечения селезеночной вены (протяженность, наличие венозных коллатералей, степень проходимости в зоне инфильтрации, наличие и локализация опухолевого и/или кровяного тромба);
5) указывается степень расширения внепеченочных желчных протоков, главного панкреатического протока с указанием уровня блока.
Рак паренхимы почки
Всем пациентам с диагнозом рак почки рекомендуется выполнять КТ брюшной полости с внутривенным контрастированием с использованием неионных йодсодержащих препаратов для оценки распространенности опухолевого процесса и планирования лечения. Пациентам с подтвержденным диагнозом почечно-клеточный рак стадии ≥ cT1b и/или cN1 рекомендуется проведение КТ органов грудной клетки.
Протокол мультидетекторной КТ включает нативную фазу, кортикомедуллярную фазу (через 40 сек. после начала введения контрастного препарата), нефрографическую фазу (через 90 сек. после начала введения контрастного препарата) и урографическую фазу (через 7 мин. после введения контрастного препарата).
Рекомендуемая толщина реконструированного среза КТ должна составлять 1–3 мм. Трехмерная КТ-реконструкция отображает анатомию сосудов почки, взаимоотношение почечной паренхимы и новообразования, а также помогает планировать хирургический доступ, объем и ход оперативного вмешательства.
Использование стандартизованных объективных и воспроизводимых нефрометрических шкал (RENAL, PADUA) нивелирует вариабельность трактовки результатов визуализации разными специалистами. Нефрометрические показатели могут предсказать ожидаемую техническую сложность резекции почки и коррелируют с длительностью ишемии, операционным временем, объемом кровопотери, частотой осложнений и вероятностью перехода от резекции почки к радикальной нефрэктомии. Нефрометрические шкалы могут помочь в принятии клинических решений в отношении объема операции и хирургического доступа.
Дифференциальная диагностика новообразований поджелудочной железы и почек в большей степени основана на оценке структуры опухоли. Кистозные и мягкотканные или солидные образования поджелудочной железы и почек требуют разного диагностического алгоритма и подхода. Например, кистозные образования почек для стратификации риска малигнизации подлежат интерпретации в соответствии с классификацией Bosniak (версия 2019).
Материал подготовила: к.м.н. Лаптева М.Г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Рис. 1. А – нативная фаза, Б – артериальная фаза, В – венозная фаза, Г – отсроченная фаза.
Мужчина, 67 лет, с диагнозом рак тела и антрального отдела желудка с метастатическим поражением печени. По данным КТ, на одном срезе в печени визуализируются три очаговых образования с различным характером контрастирования. В С2 левой доли гиподенсный очаг с четкими контурами, без признаков накопления КВ – киста. В центральных отделах С8 правой доли очаг без четких контуров, с признаками накопления КВ по периферии – метастаз. В С8 субкапсулярный очаг с гиперваскулярным характером контрастирования, в поздние фазы очаг не визуализируется на фоне контрастной паренхимы – гемангиома.
Мужчина, 67 лет, с диагнозом рак тела и антрального отдела желудка с метастатическим поражением печени. По данным КТ, на одном срезе в печени визуализируются три очаговых образования с различным характером контрастирования. В С2 левой доли гиподенсный очаг с четкими контурами, без признаков накопления КВ – киста. В центральных отделах С8 правой доли очаг без четких контуров, с признаками накопления КВ по периферии – метастаз. В С8 субкапсулярный очаг с гиперваскулярным характером контрастирования, в поздние фазы очаг не визуализируется на фоне контрастной паренхимы – гемангиома.
Рис. 2. А – нативная фаза, Б – кортикомедуллярная фаза, В – нефрографическая фаза, Г – урографическая фаза.
Мужчина, 61 год, с диагнозом светлоклеточный почечно-клеточный рак G2. Морфологическое заключение: светлоклеточный почечно-клеточный рак G2 c выраженными вторичными кистозными изменениями, кровоизлияниями, отложением солей кальция в перегородки, обширными очагами некроза (более 30% объема опухоли). По данным РКТ, в нижнем сегменте правой почки визуализируется кистозное образование с неравномерно утолщенной стенкой, на всем протяжении которой имеются включения кальцинатов по правой полуокружности образования визуализируется солидный компонент толщиной до 2,0 см с признаками накопления КВ– категория Bosniak IV.
Мужчина, 61 год, с диагнозом светлоклеточный почечно-клеточный рак G2. Морфологическое заключение: светлоклеточный почечно-клеточный рак G2 c выраженными вторичными кистозными изменениями, кровоизлияниями, отложением солей кальция в перегородки, обширными очагами некроза (более 30% объема опухоли). По данным РКТ, в нижнем сегменте правой почки визуализируется кистозное образование с неравномерно утолщенной стенкой, на всем протяжении которой имеются включения кальцинатов по правой полуокружности образования визуализируется солидный компонент толщиной до 2,0 см с признаками накопления КВ– категория Bosniak IV.
А
В
Б
Г
А
В
Б
Г








МРТ ОРГАНОВ МАЛОГО ТАЗА У ЖЕНЩИН



Рис. 1. Пациентка Ж. 45 лет. Опухоль мочевого пузыря. МРТ таза: на Т2ВИ в ортогональных проекциях (а–в) слои стенки мочевого пузыря и структуры стенок матки четко не дифферен- цируются. После введения ГМРКС маловыраженное накопление препарата в мышечном слое (г–д – 2-желтое) по сравнению со слизистой мочевого пузыря (г–д – 1-красное) позволяет визуализировать опухолевую инфильтрацию передней стенки матки (ж), что невозможно по нативным Т1 ВИ (е)
Материал подготовила: к.м.н. Лаптева М.Г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
МРТ-исследование органов малого таза следует проводить на аппаратах напряжённостью поля не менее 1,5 T с использованием мультиканальной многоэлементной приемной катушки для «тела». Стандартный протокол нативного исследования органов малого таза у женщин:
а) Сагиттальные Т2ВИ на основе импульсной последовательности Turbo Spin Echo (TSE) TSE
б) Коронарные Т2ВИ TSE
в) Аксиальные Т2ВИ TSE
г) Аксиальные Т1ВИ TSE
д) Т2ВИ TSE в наиболее информативной проекции (перпендикулярно длиннику тела или шейки матки, соответственно, при подозрении на опухоли тела или шейки матки, аксиальные или коронарные – при подозрении на опухоли яичников)
е) Т2ВИ TSE в наиболее информативной проекции с подавлением сигнала жировой ткани
ж) Диффузионно-взвешенных изображений (ДВИ, DWI) с подавлением сигнала жировой ткани (b = 50–...–600 или 800) в наибо- лее информативной проекции с подавлением сигнала жировой ткани и построением карт измеряемого коэффициента диффузии (ИКД)
з) T1ВИ на основе импульсной последовательности некогерентного градиентного эха с помощью трехмерной (3D) импульсной последовательности volumetric interpolated breath-hold sequence (3D VIBE) с подавлением сигнала жировой ткани с высоким разрешением в наиболее информативной проекции до введения МР-контрастного средства (МРКС)
и) динамическое контрастное усиление: T1ВИ на основе импульсной последовательности сверхбыстрого градиентного эхо (3D Т1ВИ TWIST) с подавлением сигнала жировой ткани в наиболее информативной проекции с последующим автоматическим (или вручную) вычитанием изображений, полученных до введения МРКС
к) 3D Т1ВИ VIBE с подавлением сигнала жировой ткани с высоким разрешением в наиболее информативной проекции после введения МРКС
При динамическом исследовании в процессе введения МРКС пациент должен размещаться на деке МР-томографа (внутри последнего), скорость введения – 2,0–3,0 мл/сек. для 0,5 молярных МРКС в дозе 0,2 мл/кг массы тела, 2,5–3,0 мл/сек. для 1,0 молярных МРКС в дозе 0,1 мл/кг массы тела. Временные параметры динамического исследования должны учитывать 16–18 сек. для достижения препаратом брюшной части аорты.
а) Сагиттальные Т2ВИ на основе импульсной последовательности Turbo Spin Echo (TSE) TSE
б) Коронарные Т2ВИ TSE
в) Аксиальные Т2ВИ TSE
г) Аксиальные Т1ВИ TSE
д) Т2ВИ TSE в наиболее информативной проекции (перпендикулярно длиннику тела или шейки матки, соответственно, при подозрении на опухоли тела или шейки матки, аксиальные или коронарные – при подозрении на опухоли яичников)
е) Т2ВИ TSE в наиболее информативной проекции с подавлением сигнала жировой ткани
ж) Диффузионно-взвешенных изображений (ДВИ, DWI) с подавлением сигнала жировой ткани (b = 50–...–600 или 800) в наибо- лее информативной проекции с подавлением сигнала жировой ткани и построением карт измеряемого коэффициента диффузии (ИКД)
з) T1ВИ на основе импульсной последовательности некогерентного градиентного эха с помощью трехмерной (3D) импульсной последовательности volumetric interpolated breath-hold sequence (3D VIBE) с подавлением сигнала жировой ткани с высоким разрешением в наиболее информативной проекции до введения МР-контрастного средства (МРКС)
и) динамическое контрастное усиление: T1ВИ на основе импульсной последовательности сверхбыстрого градиентного эхо (3D Т1ВИ TWIST) с подавлением сигнала жировой ткани в наиболее информативной проекции с последующим автоматическим (или вручную) вычитанием изображений, полученных до введения МРКС
к) 3D Т1ВИ VIBE с подавлением сигнала жировой ткани с высоким разрешением в наиболее информативной проекции после введения МРКС
При динамическом исследовании в процессе введения МРКС пациент должен размещаться на деке МР-томографа (внутри последнего), скорость введения – 2,0–3,0 мл/сек. для 0,5 молярных МРКС в дозе 0,2 мл/кг массы тела, 2,5–3,0 мл/сек. для 1,0 молярных МРКС в дозе 0,1 мл/кг массы тела. Временные параметры динамического исследования должны учитывать 16–18 сек. для достижения препаратом брюшной части аорты.
МРТ-исследования пациенток с сохраненным менструальным циклом следует проводить в I фазу менструального цикла (на 8–10 день цикла). Контрастное усиление целесообразно проводить при исследовании органов малого таза у пациенток с подозрением на опухоли матки или яичников (при отсутствии противопоказаний к введению МРКС). Отметим, что для оценки степени локальной распространенности опухолей важно, чтобы геометрия срезов разных МР-последовательностей в наиболее информативной проекции была идентичной: угол наклона срезов и их количество, толщина срезов (желательно – 3 мм), межсрезовое расстояние (желательно – 0 мм) и поле зрения (не более 280 мм).
А
Г
Е
Ж
Д
Б
В

МРТ ОРГАНОВ МАЛОГО ТАЗА ПРИ ПОДОЗРЕНИИ НА РАК ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ

Материал подготовила: к.м.н. Лаптева М.Г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Блок А. Обзорные последовательности (оценка костей таза, лимфатических узлов)
1. Аксиальные Т2-ВИ и Т1-ВИ TSE с покрытием области большого и малого таза: использование больших полей обзора (FOV 350-400), толщина среза – 5 мм с использованием расстояния между срезами.
2. Сагиттальные Т2-ВИ TSE (толщина среза – 3–4 мм, оптимальное пространственное разрешение).
3. Коронарные Т2-ВИ TSE (толщина среза – 3–4 мм, оптимальное пространственное разрешение).
4. T1ВИ 3D-T1ВИ на базе градиентного эха с подавлением сигнала от жировой ткани с высоким пространственным разрешением в наиболее информативной проекции (чаще аксиальной) до и после введения МР-контрастного средства (МРКС).
Блок Б. Прицельные последовательности: тонкие срезы с высоким пространственным разрешением с покрытием предстательной железы и области семенных пузырьков: толщина среза – не более 3 мм, расстояние между срезами отсутствует
5. Т2-ВИ TSE в косо-аксиальной проекции (перпендикулярно уретре, если позволяет анатомия предстательной железы – перпендикулярно передней стенке прямой кишки).
6. Обязательное использование дополнительной Т2-ВИ TSE с высоким пространственным разрешением в ортогональной плоскости (т. е. косо-сагиттальной или косо-корональной).
7. DWI в косо-аксиальной проекции. Для расчёта ИКД рекомендовано использование одного низкого значения b-фактора (0–100 сек./мм2) и как минимум одного высокого значение b-фактора (800–1000 сек./мм2). Обязательное получение максимального значе ния b-фактора (1400 сек./мм2 для систем с напряжённостью магнитного поля 1,5 T; 2 000 сек./мм2 – 3T-систем) путём отдельного сбора данных или использования экстраполяции низких и высоких значений b-фактора. В расчёте ИКД не рекомендовано использование максимального значения b-фактора (более 1 000 сек./мм2).
8. Динамическое контрастное усиление (ДКУ): использование 3D- T1ВИ на базе градиентного эха с подавлением сигнала жировой ткани в косо-аксиальной проекции с последующим (автоматическим или ручным) построением субтракционных изображений. Временное разрешение не более 15 с.
Принципиально важным является соблюдение парной геометрии срезов (соблюдение единого угла наклона блока срезов) при планировании косо-аксиальных изображений Т2-ВИ, DWI и ДКУ в косо- аксиальной проекции. А также соблюдение единой толщины среза (желательно не более 3 мм), межсрезового расстояния (равно 0 – отсутствует). Для облегчения интерпретации полученных изображений рекомендовано соблюдение одинакового количества срезов и поля обзора (желательно не более 240 мм).
В основе динамического контрастного усиления лежит быстрая импульсная последовательность с получением серии Т1-ВИ после внутривенного болюсного (или струйного) введения водорастворимых гадолинийсодержащих МР-контрастных средств (МРКС). Это позволяет отследить накопление и вымывание МРКС тканью по изменению МР-сигнала ткани до, во время и после введения МРКС. Для опухолевого процесса характерны повышенный ангиогенез и физиологические характеристики, отличные от таковых в нормальных тканях за счёт изменённой гистогематической проницаемости.
При проведении динамического контрастного усиления крайне желательно использование автоматических инжекторов, что позволит стандартизировать скорость введения и точно рассчитать фармакокинетические характеристики пассажа МРКС через структуры предстательной железы.
Следует подчеркнуть, что интенсивное накопление МРКС теми или иными изменениями в структуре предстательной железы само по себе не является однозначно специфическим признаком опухолевого процесса.
У пациентов после радикальной простатэктомии при биохимическом или клиническом рецидиве выполнение мпМРТ органов малого таза происходит аналогичным образом.
1. Аксиальные Т2-ВИ и Т1-ВИ TSE с покрытием области большого и малого таза: использование больших полей обзора (FOV 350-400), толщина среза – 5 мм с использованием расстояния между срезами.
2. Сагиттальные Т2-ВИ TSE (толщина среза – 3–4 мм, оптимальное пространственное разрешение).
3. Коронарные Т2-ВИ TSE (толщина среза – 3–4 мм, оптимальное пространственное разрешение).
4. T1ВИ 3D-T1ВИ на базе градиентного эха с подавлением сигнала от жировой ткани с высоким пространственным разрешением в наиболее информативной проекции (чаще аксиальной) до и после введения МР-контрастного средства (МРКС).
Блок Б. Прицельные последовательности: тонкие срезы с высоким пространственным разрешением с покрытием предстательной железы и области семенных пузырьков: толщина среза – не более 3 мм, расстояние между срезами отсутствует
5. Т2-ВИ TSE в косо-аксиальной проекции (перпендикулярно уретре, если позволяет анатомия предстательной железы – перпендикулярно передней стенке прямой кишки).
6. Обязательное использование дополнительной Т2-ВИ TSE с высоким пространственным разрешением в ортогональной плоскости (т. е. косо-сагиттальной или косо-корональной).
7. DWI в косо-аксиальной проекции. Для расчёта ИКД рекомендовано использование одного низкого значения b-фактора (0–100 сек./мм2) и как минимум одного высокого значение b-фактора (800–1000 сек./мм2). Обязательное получение максимального значе ния b-фактора (1400 сек./мм2 для систем с напряжённостью магнитного поля 1,5 T; 2 000 сек./мм2 – 3T-систем) путём отдельного сбора данных или использования экстраполяции низких и высоких значений b-фактора. В расчёте ИКД не рекомендовано использование максимального значения b-фактора (более 1 000 сек./мм2).
8. Динамическое контрастное усиление (ДКУ): использование 3D- T1ВИ на базе градиентного эха с подавлением сигнала жировой ткани в косо-аксиальной проекции с последующим (автоматическим или ручным) построением субтракционных изображений. Временное разрешение не более 15 с.
Принципиально важным является соблюдение парной геометрии срезов (соблюдение единого угла наклона блока срезов) при планировании косо-аксиальных изображений Т2-ВИ, DWI и ДКУ в косо- аксиальной проекции. А также соблюдение единой толщины среза (желательно не более 3 мм), межсрезового расстояния (равно 0 – отсутствует). Для облегчения интерпретации полученных изображений рекомендовано соблюдение одинакового количества срезов и поля обзора (желательно не более 240 мм).
В основе динамического контрастного усиления лежит быстрая импульсная последовательность с получением серии Т1-ВИ после внутривенного болюсного (или струйного) введения водорастворимых гадолинийсодержащих МР-контрастных средств (МРКС). Это позволяет отследить накопление и вымывание МРКС тканью по изменению МР-сигнала ткани до, во время и после введения МРКС. Для опухолевого процесса характерны повышенный ангиогенез и физиологические характеристики, отличные от таковых в нормальных тканях за счёт изменённой гистогематической проницаемости.
При проведении динамического контрастного усиления крайне желательно использование автоматических инжекторов, что позволит стандартизировать скорость введения и точно рассчитать фармакокинетические характеристики пассажа МРКС через структуры предстательной железы.
Следует подчеркнуть, что интенсивное накопление МРКС теми или иными изменениями в структуре предстательной железы само по себе не является однозначно специфическим признаком опухолевого процесса.
У пациентов после радикальной простатэктомии при биохимическом или клиническом рецидиве выполнение мпМРТ органов малого таза происходит аналогичным образом.
МРТ ОРГАНОВ МАЛОГО ТАЗА ПРИ ПОДОЗРЕНИИ НА ОПУХОЛИ ПРЯМОЙ КИШКИ И АНАЛЬНОГО КАНАЛА

Материал подготовила: к.м.н. Лаптева М.Г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Стандартный протокол нативного исследования органов малого таза у пациентов с подозрением на опухоли прямой кишки и анального канала:
а) Сагиттальные Т2ВИ TSE
в) Аксиальные Т2ВИ TSE
г) Аксиальные Т1ВИ TSE
д) Аксиальные DWI (b = 50–...–600 или 800) с подавлением сигнала жировой ткани и построением ИКД-карт=
е) Прицельная проекция зоны интереса Т2ВИ TSE по короткой оси опухоли (перпендикулярно оси поражённого отдела прямой кишки или анального канала)
ж) Прицельная проекция зоны интереса Т2ВИ TSE по длинной оси опухоли (параллельно оси поражённого отдела прямой кишки или анального канала)
Прицельные проекции зоны интереса следует выполнять с толщиной среза не менее 3 мм, высоким разрешением (не более 0,7х0,7 мм), малым полем обзора (160–210 мм) и высокими значениями матрицы сбора дан- ных (256–320). Опционально исследование можно дополнить аксиаль- ными/коронарными Т2ВИ TSE с подавлением сигнала жировой ткани или STIR и коронарными Т2ВИ TSE. Внутривенное контрастное усиление проводят в случаях недостаточной информативности нативной МРТ.
При интерпретации данных МРТ прямой кишки на ряду оценки распространенности самой опухоли важно отметить наличие вовле- чения мезоректальной фасции, леваторов, пуборектальной мышцы, в том числе лимфатическими узлами с признаками метастатического поражения и венозными депозитами. Именно эти характеристики влияют на выбор тактики лечения.
а) Сагиттальные Т2ВИ TSE
в) Аксиальные Т2ВИ TSE
г) Аксиальные Т1ВИ TSE
д) Аксиальные DWI (b = 50–...–600 или 800) с подавлением сигнала жировой ткани и построением ИКД-карт=
е) Прицельная проекция зоны интереса Т2ВИ TSE по короткой оси опухоли (перпендикулярно оси поражённого отдела прямой кишки или анального канала)
ж) Прицельная проекция зоны интереса Т2ВИ TSE по длинной оси опухоли (параллельно оси поражённого отдела прямой кишки или анального канала)
Прицельные проекции зоны интереса следует выполнять с толщиной среза не менее 3 мм, высоким разрешением (не более 0,7х0,7 мм), малым полем обзора (160–210 мм) и высокими значениями матрицы сбора дан- ных (256–320). Опционально исследование можно дополнить аксиаль- ными/коронарными Т2ВИ TSE с подавлением сигнала жировой ткани или STIR и коронарными Т2ВИ TSE. Внутривенное контрастное усиление проводят в случаях недостаточной информативности нативной МРТ.
При интерпретации данных МРТ прямой кишки на ряду оценки распространенности самой опухоли важно отметить наличие вовле- чения мезоректальной фасции, леваторов, пуборектальной мышцы, в том числе лимфатическими узлами с признаками метастатического поражения и венозными депозитами. Именно эти характеристики влияют на выбор тактики лечения.
МРТ КОСТНО-МЫШЕЧНОЙ СИСТЕМЫ

Материал подготовила: к.м.н. Лаптева М.Г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Диагноз саркомы костей и мягких тканей устанавливается на мультидисциплинарном консилиуме в минимальном составе: онколог (в том числе хирург-онкоортопед), рентгенолог и патоморфолог, с учётом клинических данных, данных лучевых исследований и материала, взятого при биопсии, либо послеоперационного материала (ВОЗ-2020). Выбор метода биопсии, участка и доступа также определяется на мультидисциплинарном консилиуме на основании лучевых данных, в первую очередь МРТ.
На первом этапе обследования всем пациентам с подозрением на саркому кости и мягких тканей при отсутствии абсолютных противопоказаний показано выполнение МРТ поражённого отдела. МРТ обладает наиболее высокой из всех существующих методов пространственной и тканевой визуализацией. Метод позволяет получать изображения с высочайшей тканевой специфичностью в любых выбранных проекциях. МРТ области поражения является предпочтительным методом визуализации для оценки местной распространённости.
Целями исследования являются: дифференциальная диагностика (как с неопухолевыми процессами, так и между различными нозологическими единицами злокачественных и доброкачественных опухолей), оценка местной распространённости, планирование биопсии, оценка возможности и объёма хирургического лечения, планирование лучевой терапии, оценка эффективности лекарственной и/или лучевой терапии, выявление рецидивов опухолей.
При планировании хирургического лечения МРТ должна быть выполнена в сроки не более чем за 2 месяца до операции для относительно медленно растущих опухолей, для опухолей с выраженным потенциалом роста – в сроки не более чем за 2 недели до операции. Для адекватной оценки эффективности лекарственного и лучевого лечения срок контрольной точки обследования – не более 2 недель до начала специфического лечения.
Специальной подготовки для проведения МРТ костно-мышечной системы не требуется. Желательно проведение МР-исследования до биопсии опухоли, т. к. реактивные воспалительные изменения после биопсии могут изменять МР-картину, имитируя опухолевую инфильтрацию, что осложняет установление истинных границ новообразования.
Стандартный протокол МРТ-исследования при опухолях костей и мягких тканей:
На первом этапе обследования всем пациентам с подозрением на саркому кости и мягких тканей при отсутствии абсолютных противопоказаний показано выполнение МРТ поражённого отдела. МРТ обладает наиболее высокой из всех существующих методов пространственной и тканевой визуализацией. Метод позволяет получать изображения с высочайшей тканевой специфичностью в любых выбранных проекциях. МРТ области поражения является предпочтительным методом визуализации для оценки местной распространённости.
Целями исследования являются: дифференциальная диагностика (как с неопухолевыми процессами, так и между различными нозологическими единицами злокачественных и доброкачественных опухолей), оценка местной распространённости, планирование биопсии, оценка возможности и объёма хирургического лечения, планирование лучевой терапии, оценка эффективности лекарственной и/или лучевой терапии, выявление рецидивов опухолей.
При планировании хирургического лечения МРТ должна быть выполнена в сроки не более чем за 2 месяца до операции для относительно медленно растущих опухолей, для опухолей с выраженным потенциалом роста – в сроки не более чем за 2 недели до операции. Для адекватной оценки эффективности лекарственного и лучевого лечения срок контрольной точки обследования – не более 2 недель до начала специфического лечения.
Специальной подготовки для проведения МРТ костно-мышечной системы не требуется. Желательно проведение МР-исследования до биопсии опухоли, т. к. реактивные воспалительные изменения после биопсии могут изменять МР-картину, имитируя опухолевую инфильтрацию, что осложняет установление истинных границ новообразования.
Стандартный протокол МРТ-исследования при опухолях костей и мягких тканей:
- МРТ зоны первичного опухолевого очага выполняется в положении пациента лёжа на спине либо в удобной для пациента позе при наличии болевого синдрома либо контрактур, не позволяющих провести исследование в положении на спине.
- Основным правилом является полный захват опухоли и её внекостного компонента в зону сканирования, что определяет вариабельный FOV (field of view – поле обзора) и количество срезов в каждом протоколе. При расположении опухоли в длинных и коротких костях необходим захват близлежащего сустава либо обоих близлежащих суставов при расположении опухоли в центральном отделе диафиза или массивном опухолевом поражении. Толщина среза также вариабельна – от 1 мм при очень малых размерах опухоли в мелких костях до 5 мм и более при массивных опухолях.
- Ориентация проекций проводится в зависимости от локализации опухоли – по длиннику и перпендикулярно ему в коротких и длинных костях, по оси позвоночника и крестца в осевом скелете.
- Для корректной интерпретации структуры опухоли необходимо выполнение 3 стандартных режимов МР-исследования (Т2-ВИ, Т2-ВИ с одним из типов жироподавления, Т1-ВИ), в 1 проекции с идентичными параметрами толщины среза. Для выполнения всех 3 режимов выполняется, как правило, наиболее информативная в плане оценки локализации проекция – аксиальная («пироговские срезы») – в большинстве локализаций (при расположении опухоли в позвонках, как правило, наиболее информативной будет сагиттальная проекция, в целом выбор проекций – на усмотрение рентгенолога).
- T2-ВИ выполняются минимум в 2 ортогональных плоскостях: аксиальной и 1 из продольных (чаще коронарная, в отдельных случаях, в особенности при локализации опухоли в позвонках, сагиттальная), желательно выполнение Т2-ВИ во всех 3 стандартных проекциях. Т2-ВИ и Т2-ВИ с одним из типов жироподавления по визуальным характеристикам наиболее приближены к анатомической картине при хирургическом вмешательстве, поэтому желательно выполнять данные режимы в коронарной проекции для корректной оценки хирургического поля.
- В целом минимальный достаточный объём – 5 протоколов: 3 стандартных (Т2-ВИ, Т2-ВИ с одним из типов жироподавления, Т1) в 1 проекции, Т2-ВИ и Т2-ВИ с жироподавлением – в иной ортогональной проекции. Дополнительно желательно выполнение Т2-ВИ в 3-й проекции, а также любые другие дополнительные протоколы по решению рентгенолога для оценки взаимосвязи опухоли с окружающими структурами.
- При обследовании пациентов с металлоконструкциями необходимо применение методов коррекции артефактов либо специализированных протоколов исследования.
Рис. 1. Стандартный протокол МР-обследования на примере пациента с центральной хондросаркомой правой плечевой кости. А – Т2-ВИ в коронарной проекции, Б – Т2-ВИ с жироподавлением (TIRM) в коронарной проекции, В – Т2-ВИ в сагиттальной проекции, Г – Т2-ВИ в аксиальной проекции, Д – Т2-ВИ с жироподавлением (TIRM) в аксиальной проекции, Е – Т1-ВИ в аксиальной проекции. Указаны проекционные линии ориентации срезов друг относительно друга, по оси плечевой кости
В мировой литературе нет консенсуса об однозначной необходимости либо отсутствии необходимости выполнения МР-исследований с внутривенным контрастированием при саркомах костей и мягких тканей. Решение вопроса о необходимости введения контрастного препарата остаётся за специалистами, назначающими и проводящими МР-исследование. Большинство процессов в костях и мягких тканях, как доброкачественных, так и злокачественных, характеризуются повышенным контрастированием по сравнению с окружающими тканями, поэтому в вопросах дифференциальной диагностики в большинстве случаев контрастирование не даёт дополнительной информации, при этом исследование удлиняется, становится дороже и несёт риск аллергической реакции для пациента (хотя и существенно более низкий, чем при контрастировании йодсодержащими препаратами при РКТ).
При выполнении МРТ с в/в контрастированием (препараты на основе гадолиния) рекомендовано выполнение одинаковых протоколов в режиме Т1-ВИ (предпочтительно с жироподавлением) до и непосредственно после внутривенного введения контрастного препарата, желательно выполнение не менее 2 проекций, а также построение субтракционных изображений. Однозначными показаниями к назначению внутривенного контрастирования следует считать ситуации подозрения на метастатическое поражение спинномозговых оболочек, а также выявление рецидивов опухоли малых размеров в мягких тканях.
По результатам проведённого МРТ-обследования в протоколе на основании полученных данных должны быть отражены следующие аспекты:
Большинство сарком не обладают местно-инфильтративным ростом, редко вызывают истинное прорастание окружающих структур, наиболее часто встречается экспансивное оттеснение. Критерием отсутствия вовлечения в процесс является прослеживающаяся между опухолью и сосудами/нервами/органами жировая прослойка, лучше визуализирующаяся в режиме Т1-ВИ, как правило, в аксиальной проекции. При отсутствии чёткой жировой прослойки между сосудом и опухолью критерием возможности удаления опухоли без сосудистой пластики является прилежание опухоли к сосуду менее чем на половину полуокружности.
Важно отдельно отметить техническую сложность и длительность МР-исследования костно-мышечной системы (не менее 20 мин. на одну анатомическую зону для выполнения стандартных проекций), что может быть очень проблематично для пациентов с опухолями костей и мягких тканей, многие из которых испытывают во время исследования сильную боль, связанную зачастую в том числе с вынужденным положением конечности, местной распространённостью. Всегда стоит учитывать этот момент при планировании исследования и руководствоваться принципом проведения «минимального достаточного» количества протоколов, что требует тесной совместной работы врача и лаборанта, большого опыта лаборанта, выполняющего исследование.
При выполнении МРТ с в/в контрастированием (препараты на основе гадолиния) рекомендовано выполнение одинаковых протоколов в режиме Т1-ВИ (предпочтительно с жироподавлением) до и непосредственно после внутривенного введения контрастного препарата, желательно выполнение не менее 2 проекций, а также построение субтракционных изображений. Однозначными показаниями к назначению внутривенного контрастирования следует считать ситуации подозрения на метастатическое поражение спинномозговых оболочек, а также выявление рецидивов опухоли малых размеров в мягких тканях.
По результатам проведённого МРТ-обследования в протоколе на основании полученных данных должны быть отражены следующие аспекты:
- Точная локализация выявленных изменений: для опухолей кости – отдел поражённой кости, для опухолей мягких тканей – отдел тела с указанием костных ориентиров (по возможности для всех опухолей – с указанием также расстояния от верхнего и нижнего полюсов опухоли до поверхностно определяемого костного ориентира, что будет важно для планирования объёма последующего хирургического лечения).
- Тканевая характеристика опухоли (солидный, хрящевой, кистозный, миксоидный, фиброзный, жировой компоненты, остеоид и т. д.), а также гомогенность/не гомогенность структуры опухоли (наличие кровоизлияний, зон некроза и миксоматоза, участков выпадения МР-сигнала за счёт наличия чаще оссификатов требует сопоставления с рентгенологическими методами). При введении контрастного препарата – характер и степень контрастного усиления.
- Размеры опухоли (указание 3 максимальных размеров с учётом внекостного компонента при его наличии во взаимно перпендикулярных плоскостях). Отдельно возможно описание внутрикостных размеров опухоли кости.
- Характеристика контура опухоли (чёткий, нечёткий).
- Состояние окружающих тканей (не изменены, отёчны, деформированы, экспансивное оттеснение, инфильтративный рост опухоли в окружающие ткани и т. д.).
- Состояние коркового слоя исходной и/или прилежащей кости (сохранён, разрушен, особенности характера деструкции коркового слоя: мелкоочаговая, на большом протяжении и т. д.).
- Подробная характеристика распространённости опухоли (связь с костями, мышцами, сосудистыми и нервным структурами, близлежащими органами и т. д.), оценка вовлечения суставных поверхностей костей, распространения опухоли в полость суставов.
- Наличие патологического перелома.
- Наличие других патологических изменений в зоне исследования, в первую очередь метастазов в кости и лимфатические узлы на уровне обследования, отсевов в мягкие ткани, любые другие изменения.
Большинство сарком не обладают местно-инфильтративным ростом, редко вызывают истинное прорастание окружающих структур, наиболее часто встречается экспансивное оттеснение. Критерием отсутствия вовлечения в процесс является прослеживающаяся между опухолью и сосудами/нервами/органами жировая прослойка, лучше визуализирующаяся в режиме Т1-ВИ, как правило, в аксиальной проекции. При отсутствии чёткой жировой прослойки между сосудом и опухолью критерием возможности удаления опухоли без сосудистой пластики является прилежание опухоли к сосуду менее чем на половину полуокружности.
Важно отдельно отметить техническую сложность и длительность МР-исследования костно-мышечной системы (не менее 20 мин. на одну анатомическую зону для выполнения стандартных проекций), что может быть очень проблематично для пациентов с опухолями костей и мягких тканей, многие из которых испытывают во время исследования сильную боль, связанную зачастую в том числе с вынужденным положением конечности, местной распространённостью. Всегда стоит учитывать этот момент при планировании исследования и руководствоваться принципом проведения «минимального достаточного» количества протоколов, что требует тесной совместной работы врача и лаборанта, большого опыта лаборанта, выполняющего исследование.
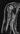




А
Г
Е
Д
Б
В

КТ КОСТНО-МЫШЕЧНОЙ СИСТЕМЫ

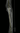
Рис. 1. Стандартный протокол РКТ-обследования на примере пациента с остеосаркомой левой большеберцовой кости. А – аксиальная проекция в костном режиме, Б – аксиальная проекция в мягкотканном режиме, В – коронарная реконструкция в костном режиме, Г – сагиттальная реконструкция в костном режиме. Указаны проекционные линии ориентации реконструкций друг относительно друга, по оси бедренной кости.
Материал подготовила: к.м.н. Лаптева М.Г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией̆ Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией̆ Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
РКТ является в первую очередь методом дополнительной визуализации в плане дифференциальной диагностики между различными костными и мягкотканными опухолями, а также не опухолевыми процессами. В отдельных случаях распространённость сарком по костным структурам также более информативно оценивать по данным РКТ, в особенности в анатомически сложных локализациях в осевом скелете: позвонки, кости таза, рёбра, кости черепа. Метод является более информативным, чем рентгенография, в визуализации участков оссификации и оценке их характера.
В связи с более низкой (по сравнению с МРТ) тканевой визуализацией, обусловленной физической основой метода, применение РКТ для оценки локальной распространённости сарком ограничено, однако в случаях невозможности выполнения МРТ (наличие абсолютных противопоказаний, тяжёлое общее состояние пациента, связанное в первую очередь с выраженным болевым синдромом) может проводиться, предпочтительно с в/в контрастированием (для более точной оценки распространённости по мягким тканям и взаимосвязи с сосудистыми структурами). При этом метод показывает более высокую информативность при оценке внутрикостной распространённости опухоли, чем внекостной.
Специальной подготовки для проведения РКТ костей и мягких тканей не требуется.
Рекомендации по проведению РКТ при саркомах костей и мягких тканей:
В связи с более низкой (по сравнению с МРТ) тканевой визуализацией, обусловленной физической основой метода, применение РКТ для оценки локальной распространённости сарком ограничено, однако в случаях невозможности выполнения МРТ (наличие абсолютных противопоказаний, тяжёлое общее состояние пациента, связанное в первую очередь с выраженным болевым синдромом) может проводиться, предпочтительно с в/в контрастированием (для более точной оценки распространённости по мягким тканям и взаимосвязи с сосудистыми структурами). При этом метод показывает более высокую информативность при оценке внутрикостной распространённости опухоли, чем внекостной.
Специальной подготовки для проведения РКТ костей и мягких тканей не требуется.
Рекомендации по проведению РКТ при саркомах костей и мягких тканей:
- РКТ зоны первичного опухолевого очага выполняется в положении пациента лёжа на спине либо в удобной для пациента позе при наличии болевого синдрома либо контрактур, не позволяющих провести исследование в положении на спине.
- Основным правилом является полный захват опухоли и её внекостного компонента в зону сканирования (что определяет вариабельную длину зоны сканирования и FOV (field of view – поле обзора)). При расположении в длинных и коротких костях необходим захват близлежащих суставов (проксимально и дистально), в позвонках захватывается полностью близлежащий сегмент для корректного подсчёта уровня поражения.
- Толщина среза – не более 5 мм с реконструкцией в более тонкие срезы.
- Сканирование выполняется в костном режиме («окне», центр «окна» – в диапазоне 400–600 HU, ширина «окна» – 2000–3000 HU), с последующим построением мультипланарных реконструкций в коронарной и сагиттальной проекциях. Построение сагиттальной и коронарной реконструкций необходимо проводить не стандартизировано, а индивидуально для каждого пациента с учётом конкретных особенностей локализации опухоли – в соотношении с длинником длинных и коротких костей, осью позвоночника. В наиболее информативной проекции (чаще – аксиальной) выполняется также построение мягкотканного режима (центр «окна» – в диапазоне 30–60 HU, ширина «окна» – 200–600 HU). При технической возможности построение реконструкций выполняется с наименьшей возможной толщиной среза (до 1 мм).
- При обнаружении большого объёма внекостного компонента, выходящего за пределы FOV, необходимо его расширение. При этом необходимо отметить, что вне зависимости от выбранного изначально FOV сканирование проводится на всю ширину гентри томографа, и при «обрезании» зон интереса при первичном сканировании возможно расширение FOV до необходимого. Это возможно только при работе с «сырыми данными» («raw data») протокола сканирования и, как правило, только на рабочей станции непосредственно томографа, поэтому проверка правильности выбранного FOV должна проводиться сразу же после сканирования в РКТ-кабинете, до момента удаления «сырых данных».
- При обследовании пациентов с металлоконструкциями необходимо включение режима коррекции артефактов на томографе при его наличии.
- В ряде случаев, в особенности для хирургического планирования, информативно построение 3D-реконструкций.
Рис. 2. РКТ-навигация при биопсии – выполнен безопасный доступ непосредственно в глубоко расположенную опухоль мягких тканей правой паховой области, в стороне от магистральных сосудистых и нервных структур.
Выполнение РКТ с внутривенным контрастированием показано, если данное исследование замещает МРТ (при невозможности его проведения) для более корректной оценки размеров и распространённости внекостного компонента опухоли, а также в отдельных случаях при планировании операций с пластикой сосудов (по поводу их опухолевой инвазии и/или тромбоза). С целью снижения лучевой и аллергической нагрузки рутинное применение в/в контрастного усиления без клинических показаний не рекомендуется, при выполнении РКТ в качестве дополнительного метода для дифференциальной диагностики введение контрастного препарата необязательно. При выполнении РКТ с в/в контрастированием обязательно предварительное нативное сканирование (до введения контрастного препарата) с целью последующей дифференциальной диагностики между участками накопления контрастного препарата и участками оссификации в опухоли.
РКТ с в/в контрастированием проводится по вышеуказанному алгоритму выбора объёма зоны сканирования и параметров сканирования. Для в/в контрастного усиления используются водорастворимые препараты на основе йода, с концентрацией не менее 300 мг/мл. Объём КВ определяется из расчёта 0,5–1,0 мл/кг веса пациента. Скорость введения КВ = 3–5 мл/сек. Необходимые фазы контрастирования: артериальная (на 15–20 сек. после начала введения контрастного препарата) и венозная фаза (на 40–45 сек.).
По результатам проведённого РКТ-обследования в протоколе на основании полученных данных должны быть отражены те же аспекты, что и по данным МРТ (указано в предыдущей главе), а также дополнительно:
Критерии вовлечения в опухолевый процесс прилежащих структур (наличие жировых прослоек, степень вовлечённости сосудов) также сохраняются.
При РКТ после проведения лечения в объёме резекции с эндопротезированием – оценка на предмет исключения ортопедических осложнений после эндопротезирования (нестабильность мышечной фиксации: вывихи, асептическая нестабильность, структурные изменения конструкции эндопротеза, перипротезные переломы).
Биопсия опухоли является ключевым моментом в постановке диагноза саркомы, на основании материала, полученного при биопсии, выполняется гистологическое исследование ткани опухоли. Наиболее предпочтительным методом получения материала является трепан-биопсия под различными видами навигационного контроля – в первую очередь под контролем РКТ (для сарком костей), реже под контролем УЗИ (предпочтительно для большинства сарком мягких тканей в связи с меньшей технической сложностью исследования и его большей доступностью), МРТ. РКТ-навигация предпочтительна при анатомически сложных локализациях, с целью взятия точной биопсии из конкретного выбранного участка опухоли, а также с целью снижения риска осложнений при биопсии. РКТ-навигация позволяет выполнить биопсию наиболее безопасно и быстро (в обход магистральных сосудистых и нервных структур, внутренних органов, точно по выбранному ранее хирургом-онкоортопедом доступу), а также точно из запланированного участка.
Манипуляция проводится хирургом в присутствии врача-рентгенолога, контролирующего особенности визуализации при процедуре, по следующему алгоритму:
РКТ с в/в контрастированием проводится по вышеуказанному алгоритму выбора объёма зоны сканирования и параметров сканирования. Для в/в контрастного усиления используются водорастворимые препараты на основе йода, с концентрацией не менее 300 мг/мл. Объём КВ определяется из расчёта 0,5–1,0 мл/кг веса пациента. Скорость введения КВ = 3–5 мл/сек. Необходимые фазы контрастирования: артериальная (на 15–20 сек. после начала введения контрастного препарата) и венозная фаза (на 40–45 сек.).
По результатам проведённого РКТ-обследования в протоколе на основании полученных данных должны быть отражены те же аспекты, что и по данным МРТ (указано в предыдущей главе), а также дополнительно:
- Характер деструкции костной ткани (литическая, смешанная, пластическая).
- Наличие в структуре опухоли включений: костной плотности (признаки костеобразования и их характеристика: по хрящевому типу, по типу остеоида и т. д.), жировой плотности, газа, участков кровоизлияний и кист.
- Характеристика контура опухоли (чёткий, нечёткий, склерозированный и т. д.).
- Состояние окружающей костной ткани (не изменена, изменена по типу разрежения/уплотнения), а также мягких тканей на уровне поражения (деформация, отёчность, экспансивное оттеснение, инфильтративный рост опухоли в окружающие ткани и т. д.).
Критерии вовлечения в опухолевый процесс прилежащих структур (наличие жировых прослоек, степень вовлечённости сосудов) также сохраняются.
При РКТ после проведения лечения в объёме резекции с эндопротезированием – оценка на предмет исключения ортопедических осложнений после эндопротезирования (нестабильность мышечной фиксации: вывихи, асептическая нестабильность, структурные изменения конструкции эндопротеза, перипротезные переломы).
Биопсия опухоли является ключевым моментом в постановке диагноза саркомы, на основании материала, полученного при биопсии, выполняется гистологическое исследование ткани опухоли. Наиболее предпочтительным методом получения материала является трепан-биопсия под различными видами навигационного контроля – в первую очередь под контролем РКТ (для сарком костей), реже под контролем УЗИ (предпочтительно для большинства сарком мягких тканей в связи с меньшей технической сложностью исследования и его большей доступностью), МРТ. РКТ-навигация предпочтительна при анатомически сложных локализациях, с целью взятия точной биопсии из конкретного выбранного участка опухоли, а также с целью снижения риска осложнений при биопсии. РКТ-навигация позволяет выполнить биопсию наиболее безопасно и быстро (в обход магистральных сосудистых и нервных структур, внутренних органов, точно по выбранному ранее хирургом-онкоортопедом доступу), а также точно из запланированного участка.
Манипуляция проводится хирургом в присутствии врача-рентгенолога, контролирующего особенности визуализации при процедуре, по следующему алгоритму:
- На первом этапе проведения биопсии проводится стандартная РКТ по описанной выше методике.
- Визуализируется заранее выбранный для биопсии участок опухоли, определяется уровень введения иглы для трепан-биопсии и её планируемый ход, выполняется предоперационная разметка на коже пациента.
- Далее короткими протоколами (зона обследования – на 5–10 мм выше и ниже предполагаемого уровнях манипуляции, толщина среза – 3 мм либо меньше) либо под контролем режима care-vision проводится контроль хода иглы до достижения выбранного для биопсии участка.
- После завершения манипуляции по показаниям возможен контроль для исключения осложнений (пневмоторакса при локализации опухоли в грудной стенке, гематомы при любой локализации). При сомнении в отсутствии осложнений возможен повторный отсроченный контроль.
В целом при невозможности проведения пациенту МРТ области поражения (при наличии абсолютных противопоказаний, а также относительных, в особенности по причине тяжёлого соматического статуса, выраженного болевого синдрома с невозможностью находиться неподвижно достаточное для проведения МРТ время – не менее 20 мин.) РКТ, в том числе с в/в контрастированием, можно считать достаточным методом для оценки локальной распространённости сарком.
В завершении следует отметить, что РКТ и МРТ в диагностике опухолевого поражения костей и мягких тканей не исключают и не заменяют друг друга. Имея разную физическую основу, методы дают различную информацию о состоянии костной ткани, дополняя друг друга.
В завершении следует отметить, что РКТ и МРТ в диагностике опухолевого поражения костей и мягких тканей не исключают и не заменяют друг друга. Имея разную физическую основу, методы дают различную информацию о состоянии костной ткани, дополняя друг друга.
А
Г
Д
Б
В




КЛАССИФИКАЦИЯ LI-RADS

Материал подготовила: к.м.н. Лаптева М.Г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Стандартный протокол нативного исследования органов малого таза у пациентов с подозрением на опухоли прямой кишки и анального канала:
а) Сагиттальные Т2ВИ TSE
в) Аксиальные Т2ВИ TSE
г) Аксиальные Т1ВИ TSE
д) Аксиальные DWI (b = 50–...–600 или 800) с подавлением сигнала жировой ткани и построением ИКД-карт=
е) Прицельная проекция зоны интереса Т2ВИ TSE по короткой оси опухоли (перпендикулярно оси поражённого отдела прямой кишки или анального канала)
ж) Прицельная проекция зоны интереса Т2ВИ TSE по длинной оси опухоли (параллельно оси поражённого отдела прямой кишки или анального канала)
Прицельные проекции зоны интереса следует выполнять с толщиной среза не менее 3 мм, высоким разрешением (не более 0,7х0,7 мм), малым полем обзора (160–210 мм) и высокими значениями матрицы сбора дан- ных (256–320). Опционально исследование можно дополнить аксиаль- ными/коронарными Т2ВИ TSE с подавлением сигнала жировой ткани или STIR и коронарными Т2ВИ TSE. Внутривенное контрастное усиление проводят в случаях недостаточной информативности нативной МРТ.
При интерпретации данных МРТ прямой кишки на ряду оценки распространенности самой опухоли важно отметить наличие вовле- чения мезоректальной фасции, леваторов, пуборектальной мышцы, в том числе лимфатическими узлами с признаками метастатического поражения и венозными депозитами. Именно эти характеристики влияют на выбор тактики лечения.
а) Сагиттальные Т2ВИ TSE
в) Аксиальные Т2ВИ TSE
г) Аксиальные Т1ВИ TSE
д) Аксиальные DWI (b = 50–...–600 или 800) с подавлением сигнала жировой ткани и построением ИКД-карт=
е) Прицельная проекция зоны интереса Т2ВИ TSE по короткой оси опухоли (перпендикулярно оси поражённого отдела прямой кишки или анального канала)
ж) Прицельная проекция зоны интереса Т2ВИ TSE по длинной оси опухоли (параллельно оси поражённого отдела прямой кишки или анального канала)
Прицельные проекции зоны интереса следует выполнять с толщиной среза не менее 3 мм, высоким разрешением (не более 0,7х0,7 мм), малым полем обзора (160–210 мм) и высокими значениями матрицы сбора дан- ных (256–320). Опционально исследование можно дополнить аксиаль- ными/коронарными Т2ВИ TSE с подавлением сигнала жировой ткани или STIR и коронарными Т2ВИ TSE. Внутривенное контрастное усиление проводят в случаях недостаточной информативности нативной МРТ.
При интерпретации данных МРТ прямой кишки на ряду оценки распространенности самой опухоли важно отметить наличие вовле- чения мезоректальной фасции, леваторов, пуборектальной мышцы, в том числе лимфатическими узлами с признаками метастатического поражения и венозными депозитами. Именно эти характеристики влияют на выбор тактики лечения.
Помимо основных диагностических принципов, представленных в таблице, выделяют также и дополнительные характеристики узловых образований в печени, которые применяются для повышения или понижения категории по усмотрению рентгенолога для повышения точности определения патологических изменений, повышения уверенности в заключении, более точного определения категории. К ним относятся:
a) умеренно повышенная интенсивность образования на Т2-ВИ;
b) ограничение диффузии (при различных факторах b-value);
c) симптом «короны», соответствующий периопухолевому неравномерному усилению в артериальную фазу сканирования;
d) мозаичная внутренняя структура узла;
e) отображение по типу «узел в узле»;
f) наличие жира и/или крови в структуре образования;
g) отсутствие накопления гепатотропного контрастного вещества в гепатобилиарную фазу сканирования.
В неоднозначных случаях рекомендовано присвоить наименьшую категорию LI-RADS из возможных.
Определение категории ответа на терапию LR-TR возможно только при наличии изображения диагностического качества.
Выделяют три категории LR-TR:
Критерии оценки эффективности лечения ГЦК LR-TR учитывают наличие жизнеспособной опухоли путём измерения активно васкуляризированных участков опухоли, накапливающих контрастное вещество в артериальную фазу сканирования (по аналогии с критериям mRECIST).
a) умеренно повышенная интенсивность образования на Т2-ВИ;
b) ограничение диффузии (при различных факторах b-value);
c) симптом «короны», соответствующий периопухолевому неравномерному усилению в артериальную фазу сканирования;
d) мозаичная внутренняя структура узла;
e) отображение по типу «узел в узле»;
f) наличие жира и/или крови в структуре образования;
g) отсутствие накопления гепатотропного контрастного вещества в гепатобилиарную фазу сканирования.
В неоднозначных случаях рекомендовано присвоить наименьшую категорию LI-RADS из возможных.
Определение категории ответа на терапию LR-TR возможно только при наличии изображения диагностического качества.
Выделяют три категории LR-TR:
- вероятно/точно нежизнеспособная опухоль – LR-TR Nonviable;
- вероятно/точно жизнеспособная опухоль – LR-TR Viable;
- в сомнительных случаях – LR-TR Equivocal.
Критерии оценки эффективности лечения ГЦК LR-TR учитывают наличие жизнеспособной опухоли путём измерения активно васкуляризированных участков опухоли, накапливающих контрастное вещество в артериальную фазу сканирования (по аналогии с критериям mRECIST).
Таблица 1. Шкала LR
Таблица 2. Диагностика образований печени по шкале LR
*Пороговое значение роста: ≥ 50% увеличение размеров образования за ≤ 6 месяцев.


КЛАССИФИКАЦИЯ O-RADS ПО ДАННЫМ МРТ

Материал подготовила: к.м.н. Лаптева М.Г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Классификация O-RADS для МРТ применяется у пациентов среднего риска без острых симптомов.
Оценка изменений в яичниках применима для женщин в пре- и постменопаузе (при аменорее более года).
В случае наличия множественных или двусторонних образований каждое образование оценивается по отдельности, тактика ведения пациентки принимается в соответствии с самой высокой категорией.
Оценка изменений в яичниках применима для женщин в пре- и постменопаузе (при аменорее более года).
В случае наличия множественных или двусторонних образований каждое образование оценивается по отдельности, тактика ведения пациентки принимается в соответствии с самой высокой категорией.
Система категоризации образований яичников O-RADS для МРТ

КЛАССИФИКАЦИЯ VI-RADS


Материал подготовила: к.м.н. Лаптева М.Г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Классификация VI-RADS (Vesicle Imaging and Data Reporting System) используется для оценки степени риска инвазии рака мочевого пузыря в мышечный слой по 5 категориям:
Итоговая классификация рака мочевого пузыря определяется на основании данных Т2-ВИ, ДВИ (с построением ИКД-карт), ДКУ с присвоением по каждой МР-последовательности категории по следующим критериям (таблица 6.1).
- VI-RADS 1: крайне маловероятна;
- VI-RADS 2: маловероятна;
- VI-RADS 3: наличие сомнительно;
- VI-RADS 4: вероятна;
- VI-RADS 5: инвазия в мышечный слой и за пределы мочевого пузыря крайне вероятна.
Итоговая классификация рака мочевого пузыря определяется на основании данных Т2-ВИ, ДВИ (с построением ИКД-карт), ДКУ с присвоением по каждой МР-последовательности категории по следующим критериям (таблица 6.1).
В случае различий в категориях по разным МР-последовательностям большую значимость в определении итоговой классификации рака мочевого пузыря имеют ДКУ и ДВИ по следующей схеме:
- VI-RADS 1 = Т2-ВИ 1 + ДВИ 1 и ДКУ 1;
- VI-RADS 2 = Т2-ВИ 2 или 3 + ДВИ 2 и/или ДКУ 2;
- VI-RADS 3 = Т2-ВИ 3 + ДВИ 3 и ДКУ 3;
- VI-RADS 4 = Т2-ВИ 3, 4 или 5 + ДВИ 4 и/или ДКУ 4;
- VI-RADS 5 = Т2-ВИ 4 или 5 + ДВИ 5 и/или ДКУ 5.
Определение категории по VI-RADS
КЛАССИФИКАЦИЯ PI-RADS

















Рис. 1. PI-RADS 1.
Рис. 2. PI-RADS 2. Участки сниженного сигнала на Т2-ВИ в периферической зоне предстательной железы слева без признаков рестрикции ДВИ. При введении МР-контрастного препарата очагов с фокальным и активным накоплением МР-контрастного препарата не выявлено.
Рис. 3. Схема оценки наличия раннего контрастного усиления при выявлении фокальных участков низкого МР-сигнала на картах ИКД, не определяющихся на DWI.
Рис. 4. PI-RADS 3. Узловое гипоинтенсивное (на Т2-ВИ) образование в периферической зоне предстательной железы слева (указано стрелкой) с участками повышения сигнала на ДВИ (без убедительных признаков рестрикции ДВИ). При введении МР-контрастного препарата признаков его фокального и активного накопления не отмечено.
Рис. 5. PI-RADS 4. Пациент И. ПСА= 25,0 нг/мл. Биопсия: аденокарцинома простаты ИГ = 8 (4 + 4).
В периферической зоне предстательной железы определяется узловое образование неоднородной структуры, с нечёткими, неровными контурами размерами 1,2х0,9 см, низкого МР-сигнала на Т2-ВИ, тесно прилежащее к капсуле, с минимальным вовлечением её. Семенные пузырьки неоднородной структуры, без явных признаков распространения процесса.
В периферической зоне предстательной железы определяется узловое образование неоднородной структуры, с нечёткими, неровными контурами размерами 1,2х0,9 см, низкого МР-сигнала на Т2-ВИ, тесно прилежащее к капсуле, с минимальным вовлечением её. Семенные пузырьки неоднородной структуры, без явных признаков распространения процесса.
Материал подготовила: к.м.н. Лаптева М.Г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Классификация PI-RADS v.2.1 используется для определения вероятности наличия клинически значимого рака предстательной железы по данным мультипараметрической МРТ. Критерии диагностики различаются в зависимости от зоны предстательной железы, в которой выявлены изменения. В предстательной железе выделяют: периферическую зону, переходную (транзиторную) зону, центральную зону и переднюю фиброзно-мускулярную строму.
Периферическая зона
Характеристика:
В норме:
Критерии злокачественности:
PI-RADS 1 (периферическая зона). Очень низкая вероятность наличия клинически значимого рака предстательной железы:
Периферическая зона
Характеристика:
- окружает центральные отделы железы на уровне верхушки и срединных отделов;
- на 70 % состоит из железистой ткани;
- источник опухолевого роста в 70–80 %;
- оценка производится на: DWI, ИКД-картах.
В норме:
- на ИКД-картах: однородный МР-сигнал высокой интенсивности;
- на Т2-ВИ: высокий МР-сигнал.
Критерии злокачественности:
- низкий МР-сигнал на ИКД-картах;
- высокий МР-сигнал на ДВИ;
- низкий МР-сигнал на Т2-ВИ;
- раннее фокальное КУ.
PI-RADS 1 (периферическая зона). Очень низкая вероятность наличия клинически значимого рака предстательной железы:
- высокий МР-сигнал на картах ИКД;
- низкий МР-сигнал на DWI.
PI-RADS 2 (периферическая зона). Низкая вероятность наличия клинически значимого рака предстательной железы:
- дополнительные участки в структуре, имеющие пониженный МР-сигнал на картах ИКД и/или повышенный МР-сигнал на DWI;
- форма участка: линейная / клиновидная.
PI-RADS 3 (периферическая зона). Подозрение на наличие клинически значимого рака предстательной железы:
® PI-RADS 4.
При выявлении фокальных участков низкого МР-сигнала на картах ИКД, не определяющихся на DWI, необходима оценка наличия раннего контрастного усиления.
- фокальные участки (отличающиеся от фона);
- существенно низкий МР-сигнал на картах ИКД или высокий МР-сигнал на DWI (но не одновременно!).
® PI-RADS 4.
При выявлении фокальных участков низкого МР-сигнала на картах ИКД, не определяющихся на DWI, необходима оценка наличия раннего контрастного усиления.
Переходная (транзиторная) зона
Характеристика:
Гиперплазия транзиторной зоны:
Характеристика:
- вокруг простатической части уретры и семявыбрасывающих протоков, выше семенного холмика;
- состоит из железистых и стромальных элементов;
- основной источник роста узлов при ДГПЖ с возрастом – 95 %;
- источник опухолевого процесса в 10–20 %;
- оценку производят на Т2-ВИ: в норме негомогенная структура;
- представляет особое внимание при негативной биопсии и с высоким ПСА.
Гиперплазия транзиторной зоны:
- негомогенная структура;
- псевдокапсула;
- вариабельный МР-сигнал на Т2-ВИ: железистые элементы обусловливают высокий МР-сигнал на Т2-ВИ; стромальные элементы: низкий сигнал на Т2-ВИ;
- интенсивное КУ;
- на DWI МР-сигнал вариабелен.
- Критерии злокачественности:
- гомогенная структура неправильной формы с нечеткими контурами;
- пониженный МР-сигнал на Т2-ВИ;
- отсутствие капсулы.
PI-RADS 1 (транзиторная зона)
Типичные узлы ГПЖ:
- чёткая капсула (в плоскостях);
- кистозные включения;
- «узел в узле».
PI-RADS 2 (транзиторная зона):
- Нетипичные узлы ГПЖ:
- Часть узла очерчена / часть нет;
- Кистозные включения;
- Узлы чётко очерчены, но низкий МР-сигнал на Т2-ВИ.
- Однородный участок незначительного снижения магнитно-резонансного сигнала между окружающими узлами гиперплазии.
PI-RADS 3 (транзиторная зона)
Зоны неоднородного, умеренно гипоинтенсивного сигнала с нечеткими контурами, включая те, которые не подходят под категории PI-RADS 2, 4 или 5.
*Если образование имеет выраженно сниженный сигнала на ИКД-карте в сочетании с выраженным повышением сигнала на ДВИ по сравнению с фоном и размер более 1,5 см
® PI-RADS 4.
PI-RADS 4 / 5 (транзиторная зона):
- линзовидная форма;
- гомогенная структура;
- «размазанный» контур (нет псевдокапсулы);
- менее 1,5 см ® PI-RADS 4;
- более 1,5 см или экстрапростатическое распространение, инвазия ® PI-RADS 5.
Центральная зона
Характеристика:
Фибро-мускулярная строма.
Характеристика:
Характеристика:
- окружает семявыбрасывающие протоки от семенного бугорка до основания железы;
- симметричная форма;
- на 25 % состоит из железистой ткани, в остальном – фиброзно-мышечные элементы.
- низкий МР-сигнал на Т2-ВИ;
- низкий МР-сигнал на ИКД-картах;
- не отмечается повышения МР-сигнала на DWI;
- нет раннего КУ (обусловлено отсутствием плотной сосудистой сети);
- симметричная.
Фибро-мускулярная строма.
Характеристика:
- вентральный отдел железы на уровне основания и срединных структур;
- состоит из мышечной ткани (не является источником роста опухоли).
Рис. 6. PI-RADS 5. Узловое образование (указано стрелкой) в периферической зоне предс- тательной железы слева, размером более 15 мм. Образование гипоинтенсивно на Т2-ВИ, с признаками рестрикции ДВИ (высокий сигнал на ДВИ (b = 1400) и низкий сигнал на ИКД). При введении МР-контрастного препарата отмечается его фокальное и активное на- копление вышеописанным образованием в ранние фазы контрастирования.
Рис. 7. PI-RADS 5. Пациент М. ПСА= 20,09 нг/мл. Биопсия: аденокарцинома простаты ИГ = 7 (3 + 4). Структура железы неоднородна. Зональная дифференцировка нарушена. В периферической зоне предстательной железы справа определяется участок ограничения диффузии размером до 1,8 см, который широко прилежит к капсуле предстательной железы без достоверного выхода за её пределы. Нельзя исключить распространение на переходную зону.
Рис. 8. PI-RADS 5. Экстрапростатический/инвазивный рост. Структура железы выраженно неоднородна. Зональная структура железы нарушена. Практически вся структура предстательной железы выполнена опухолью неоднородной структуры, с инфильтрацией капсулы, семенных пузырьков, мезоректальной фасции, прямой кишки, мочевого пузыря. После введения МР-контрастного вещества в вышеописанных очагах отмечается несколько раннее активное накопление МРКС.
Рис. 11. PI-RADS 3. Структура железы выраженно неоднородна. Зональная дифференцировка сохранена. Отмечается пролабирование предстательной железы в мочевой пузырь в области воронки уретры до 3,3 см. В переходной зоне предстательной железы определяются множественные инкапсулированные узлы железисто-стромальной гиперплазии с наличием участков неоднородного, умеренно гипоинтенсивного сигнала с нечёткими контурами, без достоверных признаков уплотнения, с максимальным размером узла до 1,9 1,6 см. При введении МР-контрастного препарата отмечается его умеренное и постепенное накопление этими узлами.
Рис. 12. PI-RADS 5. Экстрапростатическое распространение
Рис. 13. Схема оценки очага в транзиторной зоне на Т2-ВИ
Рис. 14. Фибро-мускулярная строма
Рис. 10. Гиперплазия транзиторной зоны предстательной железы.
Рис. 9. Схема оценки очага в периферической зоне на DWI
PI-RADS 5 (периферическая зона). Высокая вероятность наличия клинически значимого рака предстательной железы:
- фокальные участки существенно низкого МР-сигнала на картах ИКД и высокого МР-сигнала на DWI;
- размеры участка более 1,5 см (в наибольшем измерении);
- очевидный экстрапростатический/инвазивный рост.
PI-RADS 4 (периферическая зона). Вероятно наличие клинически значимого рака предстательной железы:
- фокальные участки существенно низкого МР-сигнала на картах ИКД и высокого МР-сигнала на DWI(одновременно);
- размеры участка до 1,5 см.
В норме:
- низкий МР-сигнал на Т2-ВИ, ИКД-картах;
- гомогенная структура;
- нет повышения МР-сигнала на DWI;
- нет раннего КУ.
- высокий МР-сигнала на DWI;
- на Т2-ВИ сигнал выше, чем от скелетных мышц;
- раннее КУ.






КЛАССИФИКАЦИЯ BI-RADS ПО ДАННЫМ МРТ



BI-RADS 5. Крайне высокая вероятность злокачественности
Подобные образования имеют вероятность злокачественности более 95 %. Выполнение чрескожной биопсии необходимо для разработки индивидуальной лечебной тактики.
Подобные образования имеют вероятность злокачественности более 95 %. Выполнение чрескожной биопсии необходимо для разработки индивидуальной лечебной тактики.









Рис. 2. Киста молочной железы
Рис. 1. Импланты молочных желёз
Рис. 3. Фиброаденома
Рис. 5. Фиброаденома
Рис. 10. Рак молочной железы
Рис. 11. Рак молочной железы
Рис. 8. Гиперинтенсивное образование неправильной формы с лучистыми контурами. Рак молочной железы.
Рис. 9. Гиперинтенсивное образование неправильной формы с кольцевидным типом контрастирования. Рак молочной железы.
Рис. 7. Асимметричная сегментарная зона усиления интенсивности сигнала.
Внутрипротоковый рак
Внутрипротоковый рак
Рис. 6. Рак молочной железы
Рис. 4. Интрамаммарный л/у
Материал подготовила: к.м.н. Лаптева М.Г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
BI-RADS 0. Необходимы дополнительные исследования.
Эта категория правомерна, если выполненное исследование низкого качества или нет динамических кривых контрастирования.
В качестве рекомендуемых дополнительных исследований могут применяться повторная МРТ с надлежащим уровнем качества, ММГ, УЗИ, информация о предыдущих исследованиях.
BI-RADS 1. Отрицательная
Образования и зоны патологического контрастирования не выявлены.
BI-RADS 2. Доброкачественные структуры
Определяемые при исследовании структуры без признаков злокачественного образования:
Эта категория правомерна, если выполненное исследование низкого качества или нет динамических кривых контрастирования.
В качестве рекомендуемых дополнительных исследований могут применяться повторная МРТ с надлежащим уровнем качества, ММГ, УЗИ, информация о предыдущих исследованиях.
BI-RADS 1. Отрицательная
Образования и зоны патологического контрастирования не выявлены.
BI-RADS 2. Доброкачественные структуры
Определяемые при исследовании структуры без признаков злокачественного образования:
- гиализированные фиброаденомы, не накапливающие контрастный препарат;
- кисты;
- образования с включением жировой ткани (олеогранулёма, липома, гамартома, галактоцеле);
- импланты молочных желёз;
- послеоперационные рубцовые изменения без накопления контрастного препарата.
BI-RADS 3. Вероятно доброкачественные структуры – рекомендовано повторное исследование через 6 месяцев
Риск злокачественности составляет менее 2 %. Структура должна обладать крайне высокой вероятностью доброкачественности. Категория уместна только после проведения всех возможных дополнительных исследований (ММГ, УЗИ).
Данные считаются стабильными, если при обследовании пациента с интервалом 6 месяцев на протяжении 2 лет изменений не происходит.
Риск злокачественности составляет менее 2 %. Структура должна обладать крайне высокой вероятностью доброкачественности. Категория уместна только после проведения всех возможных дополнительных исследований (ММГ, УЗИ).
Данные считаются стабильными, если при обследовании пациента с интервалом 6 месяцев на протяжении 2 лет изменений не происходит.
BI-RADS 4. Подозрение на злокачественное образование – рекомендовано выполнение биопсии
К этой категории относятся структуры, которые не обладают всеми признаками рака молочной железы, однако имеют небольшую или умеренную вероятность (2–95 %) злокачественности. Деление на субкатегории в настоящее время признано нецелесообразным.
К этой категории относятся структуры, которые не обладают всеми признаками рака молочной железы, однако имеют небольшую или умеренную вероятность (2–95 %) злокачественности. Деление на субкатегории в настоящее время признано нецелесообразным.
BI-RADS 6. Гистологически подтверждённое злокачественное образование
К данной категории относят образования молочной железы, злокачественный характер которых морфологически доказан. Используется для проведения повторных исследований, оценки эффективности неоадъювантного лечения. Категория BI-RADS 6 не используется после проведённого хирургического лечения. При отсутствии признаков рецидива исследование классифицируется в зависимости от выявленных послеоперационных изменений как BI-RADS 2 или 3. Если имеются признаки резидуального опухолевого образования – как BI-RADS 4 или 5.
К данной категории относят образования молочной железы, злокачественный характер которых морфологически доказан. Используется для проведения повторных исследований, оценки эффективности неоадъювантного лечения. Категория BI-RADS 6 не используется после проведённого хирургического лечения. При отсутствии признаков рецидива исследование классифицируется в зависимости от выявленных послеоперационных изменений как BI-RADS 2 или 3. Если имеются признаки резидуального опухолевого образования – как BI-RADS 4 или 5.
КЛАССИФИКАЦИЯ RECIST 1.1

Материал подготовила: к.м.н. Лаптева М.Г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
Источник: Стандарты УЗИ, РКТ, МРТ, ОФЭКТ, ПЭТ/КТ и АГ исследований в онкологии. Под редакцией Б.И. Долгушина и И.Е. Тюрина. Б.И. Долгушин, И.Е. Тюрин, А.Б. Лукьянченко, Б.М. Медведева, Е.Л. Дронова и соавт. Тех. редактор: М.Г. Лаптева. 2024г.
В 2000г. EORTC, NCI и национальным исследовательским институтом Канады были созданы критерии ответа солидных опухолей — Response Evaluation Criteria In Solid Tumors (RECIST) 1.0, которые были пересмотрены на основе выборки пациентов большей репрезентативности в 2008г. с созданием RECIST 1.1. Для оценки рекомендуется использовать данные КТ или МРТ в аксиальной проекции с толщиной среза не более 5 мм, выполненных до и после внутривенного введения контрастного препарата. Применение рентгенографии грудной клетки и УЗИ не рекомендуется по причине слабой воспроизводимости.
В основе RECIST 1.1. лежит разделение поражений на измеряемые и неизмеряемые. К измеряемым относятся объёмные образования с максимальным диаметром более 10 мм и лимфатические узлы более или равные 15 мм по короткой оси. Не следует измерять остеобластические очаги в костях (возможна количественная оценка только мягкотканного компонента остеолитических очагов), кистозные образования, поражения, которые подвергались лучевому лечению. Неизмеряемые поражения включают патологические очаги максимальным диаметром менее 10 мм, лимфатические узлы от 10 мм до 14 мм по короткой оси, лептоменингеальные метастазы, асцит, плевральный и перикардиальный выпот, лимфогенный канцероматоз, органомегалию.
Среди измеряемых очагов необходимо определить не более 5 целевых (но не более 2 в одном органе), подходящих для количественной оценки. Рекомендуется выбор наибольших образований, измерение которых наиболее воспроизводимо. В аксиальной проекции следует провести максимальный продольный диаметр образования, включая кольцо периферического контрастного усиления, или короткую ось поражённых лимфатических узлов. Если целевой очаг распадается на отдельные фрагменты, рассчитывают сумму самых длинных диаметров образовавшихся фрагментов. И наоборот, если поражения сливаются, измеряют только самый длинный диаметр слившегося поражения.
При определении динамики заболевания используется «сумма наибольших размеров» всех выбранных ранее измеряемых целевых очагов, а также качественная оценка измеряемых нецелевых очагов и неизмеряемых поражений со следующей градацией ответа:
При неизменном тренде (например, при первом контрольном исследовании сумма размеров целевых очагов уменьшилась и при втором – уменьшилась) сравнение следует производить с исходной точкой (первым исследованием), в случае изменения тренда (например, при первом контрольном исследовании сумма размеров целевых очагов уменьшилась, а при втором увеличилась) – с точкой наименьших измерений.
RECIST 1.1 являются «золотым стандартом» оценки эффективности противоопухолевого лечения, однако они имеют ряд ограничений, не допускающих их применение при некоторых нозологиях, таких как лимфомы, опухоли головного мозга, гепатоцеллюлярный рак и гастроинтестинальные стромальные опухоли.
В основе RECIST 1.1. лежит разделение поражений на измеряемые и неизмеряемые. К измеряемым относятся объёмные образования с максимальным диаметром более 10 мм и лимфатические узлы более или равные 15 мм по короткой оси. Не следует измерять остеобластические очаги в костях (возможна количественная оценка только мягкотканного компонента остеолитических очагов), кистозные образования, поражения, которые подвергались лучевому лечению. Неизмеряемые поражения включают патологические очаги максимальным диаметром менее 10 мм, лимфатические узлы от 10 мм до 14 мм по короткой оси, лептоменингеальные метастазы, асцит, плевральный и перикардиальный выпот, лимфогенный канцероматоз, органомегалию.
Среди измеряемых очагов необходимо определить не более 5 целевых (но не более 2 в одном органе), подходящих для количественной оценки. Рекомендуется выбор наибольших образований, измерение которых наиболее воспроизводимо. В аксиальной проекции следует провести максимальный продольный диаметр образования, включая кольцо периферического контрастного усиления, или короткую ось поражённых лимфатических узлов. Если целевой очаг распадается на отдельные фрагменты, рассчитывают сумму самых длинных диаметров образовавшихся фрагментов. И наоборот, если поражения сливаются, измеряют только самый длинный диаметр слившегося поражения.
При определении динамики заболевания используется «сумма наибольших размеров» всех выбранных ранее измеряемых целевых очагов, а также качественная оценка измеряемых нецелевых очагов и неизмеряемых поражений со следующей градацией ответа:
- Полный ответ: отсутствие всех целевых и нецелевых очагов и лимфатических узлов >10 мм по короткой оси;
- Частичный ответ: ≥ 30 % уменьшение суммы наибольших размеров целевых очагов;
- Прогрессирование: > 20 % (и при этом не менее чем на 0,5 см) увеличение суммы наибольших размеров целевых очагов, появление новых опухолевых образований или однозначное прогрессирование нецелевых поражений;
- Стабилизация: все прочие случаи.
При неизменном тренде (например, при первом контрольном исследовании сумма размеров целевых очагов уменьшилась и при втором – уменьшилась) сравнение следует производить с исходной точкой (первым исследованием), в случае изменения тренда (например, при первом контрольном исследовании сумма размеров целевых очагов уменьшилась, а при втором увеличилась) – с точкой наименьших измерений.
RECIST 1.1 являются «золотым стандартом» оценки эффективности противоопухолевого лечения, однако они имеют ряд ограничений, не допускающих их применение при некоторых нозологиях, таких как лимфомы, опухоли головного мозга, гепатоцеллюлярный рак и гастроинтестинальные стромальные опухоли.








